Volpato, A., Ollech, D., Alvelid, J., Damenti, M., Müller, B., York, A.G., Ingaramo, M., Testa, I. “Extending fluorescence anisotropy to large complexes using reversibly switchable proteins.” Nature Biotechnology 2023, 41, 552–559. https://doi.org/10.1038/s41587-022-01489-7
分子複合体の形成や局所環境の変化を検出する手法として、蛍光異方性測定は生命科学分野で広く利用されている。回転拡散は分子の大きさや周囲の粘度に関する直接的な情報を与えるため、分子間相互作用の解析に有用である。特に時間分解蛍光異方性法は、蛍光寿命(通常1〜5ナノ秒)の時間窓内で分子の配向変化を追跡できることから、創薬や低分子結合解析において高い処理能力と分子特異性を実現している。
しかし、従来の時間分解蛍光異方性法では、観測可能な時間窓が蛍光寿命に制限されるため、約30キロダルトンを超える大型分子複合体の回転運動を検出できないという根本的な制約があった。ヒトの全タンパク質およびその複合体の大部分はこの質量範囲を超えており、従来手法では静止状態と区別できなかった。
そこで、本研究ではSTARSS法を開発し、可逆光スイッチング蛍光タンパク質(rsEGFP2やDronpaM159T)の長寿命ON-OFF状態遷移を利用することで、観測時間窓をマイクロ秒からミリ秒領域まで拡張した。これにより検出可能な質量範囲は従来の約1000倍以上に拡大し、30〜100ナノメートル径のシリカビーズの回転拡散を明確に分離できた。生細胞内ではクロマチン繊維の柔軟性、HIV-1粒子の成熟状態、Arc蛋白質のオリゴマー形成を検出することに成功した。実験系にはCobolt社製の405 nmおよび488 nm変調連続波レーザーを用い、偏光制御による光選択と蛍光読み出しを実現した。
※この要約は、オープンアクセス論文(CC BY 4.0)に基づいています。
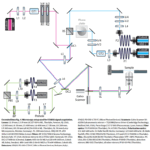
超解像顕微鏡法で使用された405nmと488nmレーザー
その他の論文要約はCobolt論文検索ページをご覧ください。


